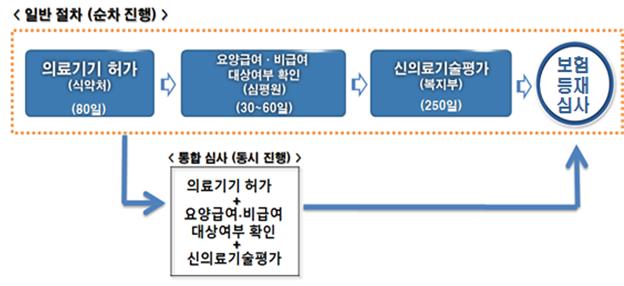
의료기기 허가 진행 중에도 급여·비급여 대상 여부 확인과 신의료기술평가를 동시에 받을 수 있게 됐다. 보건복지부(장관 박능후)와 식품의약품안전처(처장 김강립)는 10일 ‘통합심사 전환제’를 시행한다고 밝혔다.
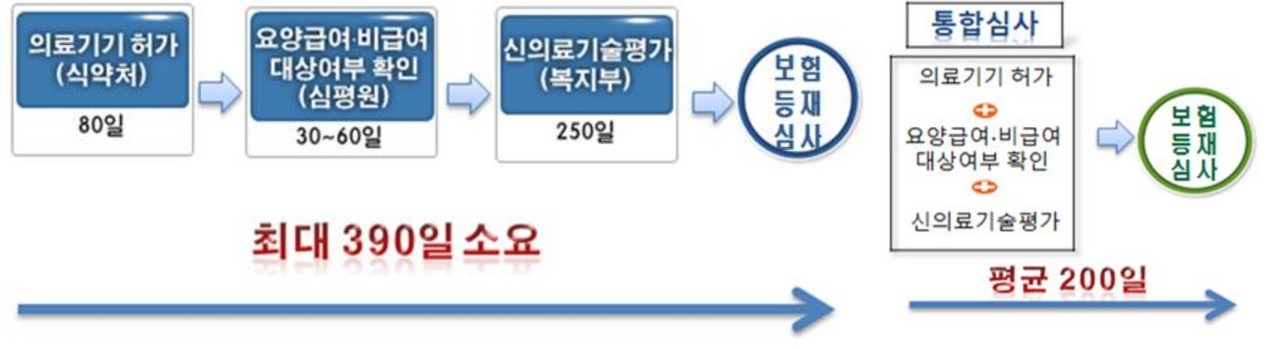
통합심사는 의료기기 시장진입 기간을 단축하기 위해 단계별로 거쳐야 했던 과정들을 병렬적으로 동시에 진행할 수 있도록 창구를 식약처로 일원화하는 제도로 2016년 7월 29일부터 시행됐다. 통합심사 신청 시 ①의료기기 허가(식약처) ②급여·비급여 대상 여부(건강보험심사평가원) ③신의료기술평가(보건의료연구원) 심사가 동시에 진행된다.
기존 통합심사는 의료기기 허가 신청 시 요양(비)급여 대상 여부 심사와 신의료기술평가 자료를 동시에 제출하는 경우에만 통합심사 신청이 가능했다. 이번 고시 개정으로 금일부터는 의료기기 허가 신청 후 심사 진행 중에도 통합심사를 신청할 수 있다.
또한 이번 개정으로 ‘체외진단의료기기법’에 따른 체외진단의료기기도 통합운영 제도 신청 대상에 포함됐다. 통합심사 운영 안정화를 위한 신의료기술평가위원회 참석가능 대상을 확대하고, 각 단계별 통합운영 중단사유 발생 시 각 기관의 불필요한 업무 방지를 위한 안정적 종료가 이루어질 수 있도록 개선하기도 했다.
보건복지부와 식품의약품안전처는 “이번 개정을 통해 의료기기 시장 진입을 위한 만반의 준비를 갖춘 업체들이 보다 편리하게 통합심사를 신청할 수 있을 것”이라며 “의료기기 업체들의 시장진입 기간이 단축될 것으로 전망된다”고 전했다.